多菌灵(CBD)被广泛用作增加农作物产量和减少病虫害的辅助工具。但是,这些工具中有些具有毒素且易于迁移,过度使用会导致环境中长期积累,从而造成环境污染。目前,影响比较严重的有地表水,土壤和地下水源,这对饮用水造成了严重的影响。多菌灵的化学性质非常稳定,在土壤和水中的半衰期为2-14周。值得注意的是,它可能导致一系列环境问题。这项工作的主要目的是研究含氧官能团对多菌灵吸附到活性炭上的影响,然后推导在某些条件下可能的吸附机理。
不同热解温度下活性炭的特性
活性炭随着热解温度的升高,C的含量增加,H和O的含量下降,N含量相对稳定。对于这几种活性炭,由于纤维素,半纤维素,木质素和其他成分的原料经过脱水,脱羧反应和脱羟基反应的热解过程,(O+N)/C和O/C的比率降低。H/C原子比也降低,表明在热解过程中形成了新的不饱和烃或芳香环结构,使活性炭更加致密。灰分含量也随着热解温度的升高而增加。活性炭样品的极性指数(O+N)/C和O/C原子比相对于其他样品有一定的降低,这表明添加甲醇和甲醛可以成功掩盖极性官能团在活性炭上。
多菌灵在活性炭上的吸附等温线
多菌灵在活性炭上的吸附等温线示于图1,随着活性炭中含O官能团的减少,N值从0.507降低至0.273,这表明活性炭中的玻璃态,硬质或凝聚态吸附域更加不均一和较宽的吸附位能分布。所有活性炭的K d值样品随着CBD浓度的增加而显着下降。造成这种情况的最可能原因是活性炭上的CBD吸附是非线性的,而活性炭上的高能吸附位被CBD占据。在较低的CBD浓度范围内,K d值随含O官能团的减少而增加。然而,在高浓度的CBD(例如1000mg L-1)下不是这种情况。结果表明,CBD在活性炭上的吸附能力取决于CBD浓度。在该实验中,极性指数(O + N)/ C原子比与低浓度下的K d值之间存在显着的负相关性,表明活性炭上更多的表面官能团限制了CBD在其表面上的吸附,并且疏水反应在活性炭上的CBD吸附中起重要作用。但是,极性指数(O+N)/C原子比与K d之间没有相关性。浓度高时,表明吸附受其他机理控制。
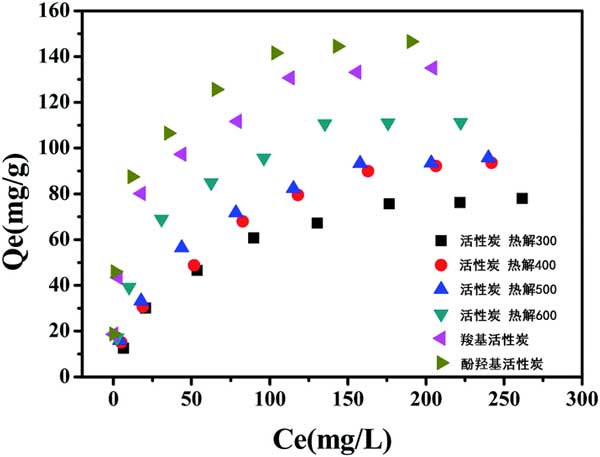
图1:活性炭对CBD的吸附等温线。
多菌灵在活性炭上的吸附动力学
活性炭上的多菌灵吸附动力学如图2所示。从图中可以看出,活性炭上多菌灵的吸附量和CBD的量在与CBD接触的前5分钟内迅速增加,达到总吸附量的80%。这是因为在初始阶段较高的驱动力导致多菌灵迅速转移至吸附剂颗粒的表面部位。5分钟后,吸附速率缓慢增加直至达到平衡。这主要是由于吸附剂上空位的减少以及固体表面上的溶质分子与本体相中的溶质分子之间的排斥。基于在该实验中制备的测试材料,值得注意的是,前5分钟的吸附量可以达到总吸附量的80%,这表明活性炭是理想的吸附剂。此外,在所有选定的CBD吸附样品中,带羧基的活性炭的吸附性能最佳。
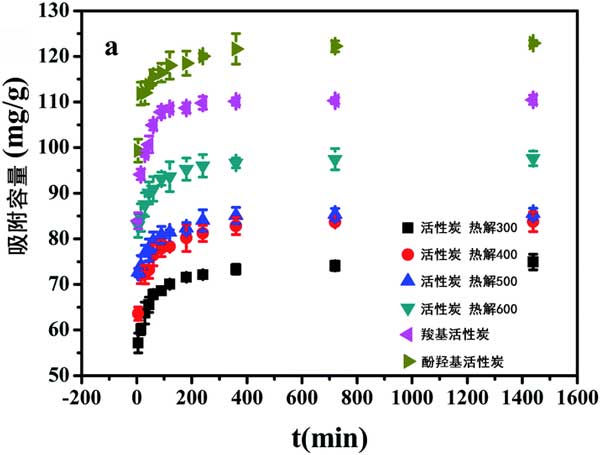
图2:CBD吸附接触时间对活性炭的影响。
多菌灵在活性炭样品上的吸附机理
大量研究表明,有机污染物在水介质上的吸附包括分配和吸附作用。为了评估在活性炭上吸附化合物时在碳化相中的吸附和在非碳化相中的分配的贡献,双模式模型在该研究领域中被成功引用。通过双模式模型计算了多菌灵在不同浓度的活性炭上的分配和吸附。在该实验中,双模型为所有样品的等温线提供了良好的拟合(图3)。在本研究中,所有活性炭上多菌灵的吸附均大于分配所有多菌灵浓度的吸附。但是,随着多菌灵浓度的增加,分配(Q p)和吸附(Q ad)对总吸附的贡献也不同。在低浓度范围内,吸附大于在活性炭上的分配,并且Q ad值贡献超过总吸附的97%。但是,在高浓度范围内,多菌灵对不同样品在整体吸附中的分配和吸附的贡献不同。当多菌灵的浓度达到300 mg L-1时在热解300、400、500摄氏度的活性炭上,吸附对总吸附的贡献仍然远远大于分配作用。尽管活性炭中含O官能团的含量逐渐减少,但分配对总吸附的贡献率却逐渐增加,特别是对于羧基活性炭和酚羟基活性炭,它们的Q p值分别达到39.4%和44.13%。主要原因可能是样品表面上含O官能团的减少导致更好地暴露于样品表面和多菌灵浓度增加,从而导致吸附过程饱和。因此,多菌灵可以分配给非碳化相。
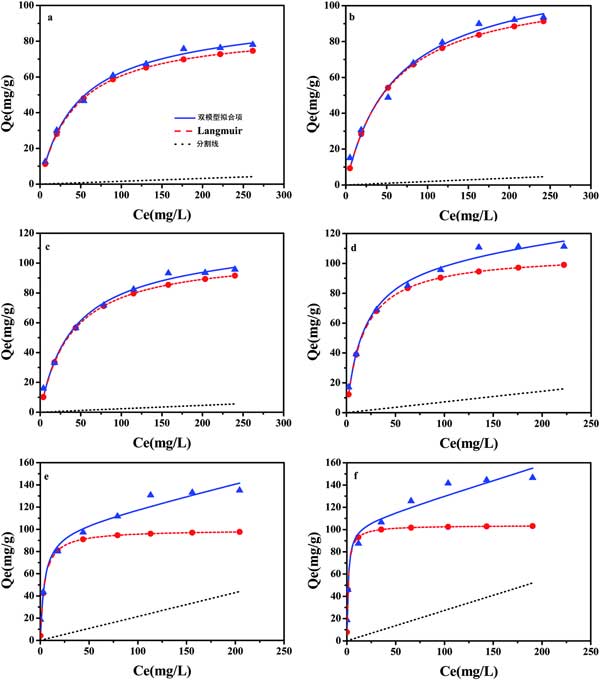
图3:通过双模型吸附模型拟合的活性炭吸附多菌灵等温线。
这项研究表明,在选定的CBD浓度下,CBD吸附对活性炭的主要贡献是一种分配机制。另外,在低浓度范围内,CBD的吸附量大于活性炭的分配量。相反,在高浓度范围内,当活性炭上的含O官能团明显降低,分配对总体吸附的影响逐渐增加。结果表明,在不同的初始pH值和不同的CBD浓度下,存在不同的吸附机理。在较低的初始pH值下,静电相互作用比疏水相互作用起着更重要的作用。但是,随着初始pH值的增加,疏水相互作用在CBD的吸附中占很大比例。因此,结果表明,这次制成的活性炭可用于高效且环保的吸附剂,以减少在水性环境中有机物的污染。